
Depozit ve Kontrolü
Nisan 4, 2024
Depozit ve Kontrolü
Mayıs 30, 2024Bakır neden önemlidir?
- İmalat ve birleştirme kolaylığı,
- Yüksek ısı transfer yetenekleri
- Cu : 325 Kcal/m,h,°C
- MS : 38,5 Kcal/m,h,°C
- Tuzlu çözeltilere, alkali çözeltilere ve organik kimyasallara karşı direnç
- Biyolojik kirlenmeye karşı direnç
- Transfer boruları genellikle çelik borulardan çok daha incedir
- Ekipman ömrü
- Tatlı suda tipik korozyon hızı: 1-3 mpy
- Klorlama sırasında oranlar 20 mpy’yi aşabilir
- Çukurlaşma(Pitting) saldırısı
- Yumuşak çeliğe galvanik saldırı
- Toksik deşarj
- Bakır oldukça zehirli bir ağır metaldir. Korozyon oranı Cu : 1 mpy
- Kondenser yüzeyi : 10.000 m² –> 6.3 kg Cu/gün
- mpy * 0.0705 * s.g. = Cu (g, m2/day) s.g. = 8.91
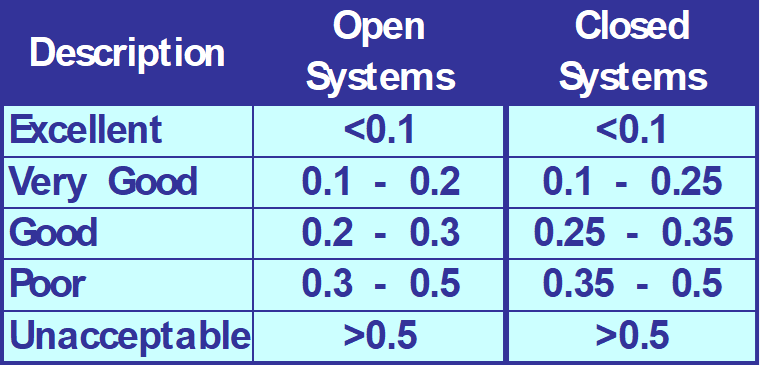
Çalışan Sistemlerde Korozyon Hızları (mpy)
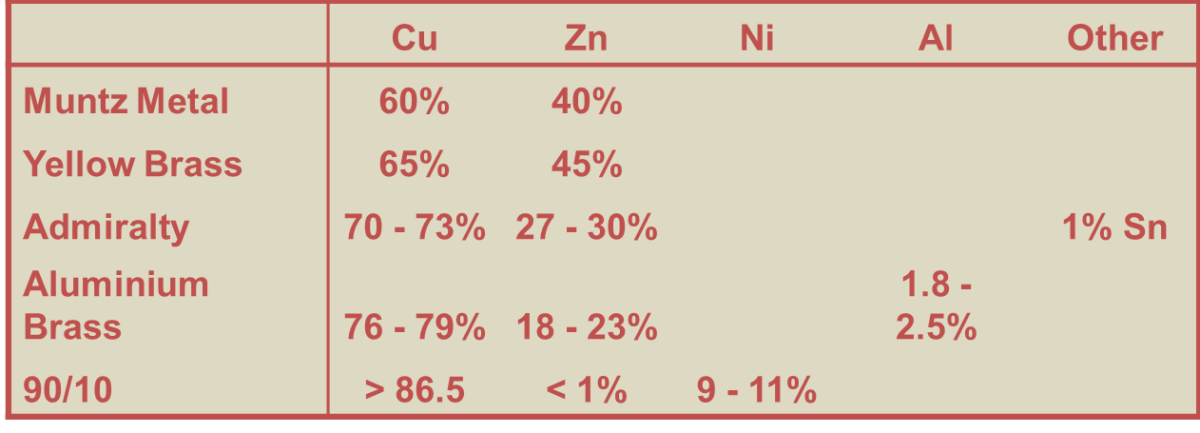
Bakır Alaşımlar
- Pirinçler : (Cu/Zn)
- Bronzlar : (Cu/Sn)
- Bakır nikel : (Cu/Ni)
Pirinçler (%40’a kadar Zn)
Galvanik Korozyon
- Korozyon potansiyeli Cu alaşımları:
- – 0,2 ila 0,4 V
- Çinko veya Alüminyum İlaveleri
- Daha anodik
- Kalay veya Nikel
- Daha katodik
- Çinkosuzlaştırma : Çinkonun uzaklaştırılması
- Cu kaplama
Bakır ve Klorür / pH
- Sentezlenmiş Deniz suyu üzerinde;
- Cl– <100 ppm pH 7.5 —> 0.5 – 4 mpy
- Cl– <100 ppm pH 6.5 —> ca. 25 mpy
- Cl– ~1000 ppm pH 7.0 –> ca. 5 mpy
- Cl– ~1500 ppm pH 8.0 –> >20 mpy (başlangıç)
- Cl– ~1500 ppm pH 8.0 –> 1-3 mpy (korozyon ürünü filmin oluşumu)
- 0.1 – 0.2 ppm serbest klor -> 1 – 10 mpy
- 0.3 – 0.5 ppm serbest klor -> 10 – 25 mpy
- 1+ ppm serbest klor –>25 mpy
Bakır ve Amonyak
- Anot
- Cu + 4NH3 –> Cu(NH3)42+ + 2e–
- Katot
- Cu(NH3)42+ + 2e– –>CuO2 + 2NH4+ + 6NH3
- Korozyon hızı 2N NH4OH çözeltisinde @ 25 °C yaklaşık 6 mm/y
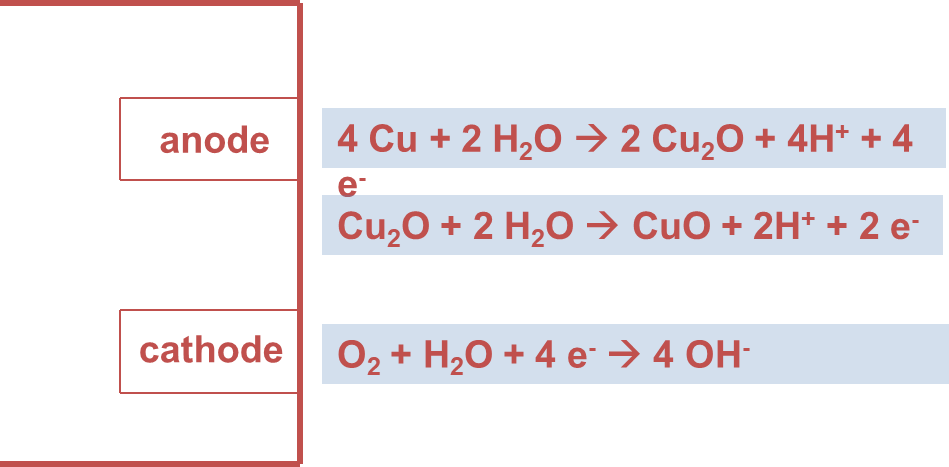
Bakır Korozyonunun Mekanizması
- Metal/oksit ara yüzünde koruyucu bakır oksit (Cu2O) filminin oluşumu – (içe doğru büyür.)
- Bakır(I)Oksit (Cu2O) oksitlenerek Bakır(II)Oksit ‘e (CuO) dönüşür.
- Bakır(II)Oksit, Bakır(I)Oksit ‘e göre daha çözünebilir yapıdadır.
- Cu2O filmi koruyucudur.
- Agresif türler Cu2O saldırarak koruyucu olmayan depozitleri (–Cl–, SH–, CN–, NH3, NO3, SO4) oluştururlar.
- pH > 8 bazik bakır tuzlarını oluşturur. CuCl2. 3Cu(OH)2 ya da CuCO3. Cu(OH)2
- Oksitleyiciler koruyucu özelliği olmayan CuO oluşumunu hızlandıracaktır.
- Bakır(I)Oksit kalınlığı genel korozyonu kontrol eder.
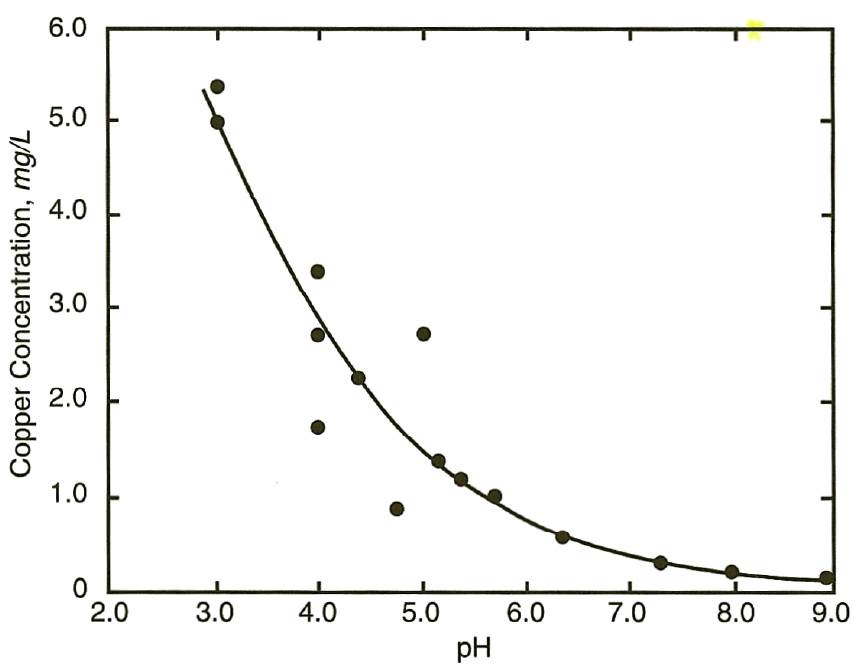
Bakır Korozyonu – pH
Bakır Korozyonu – Hız
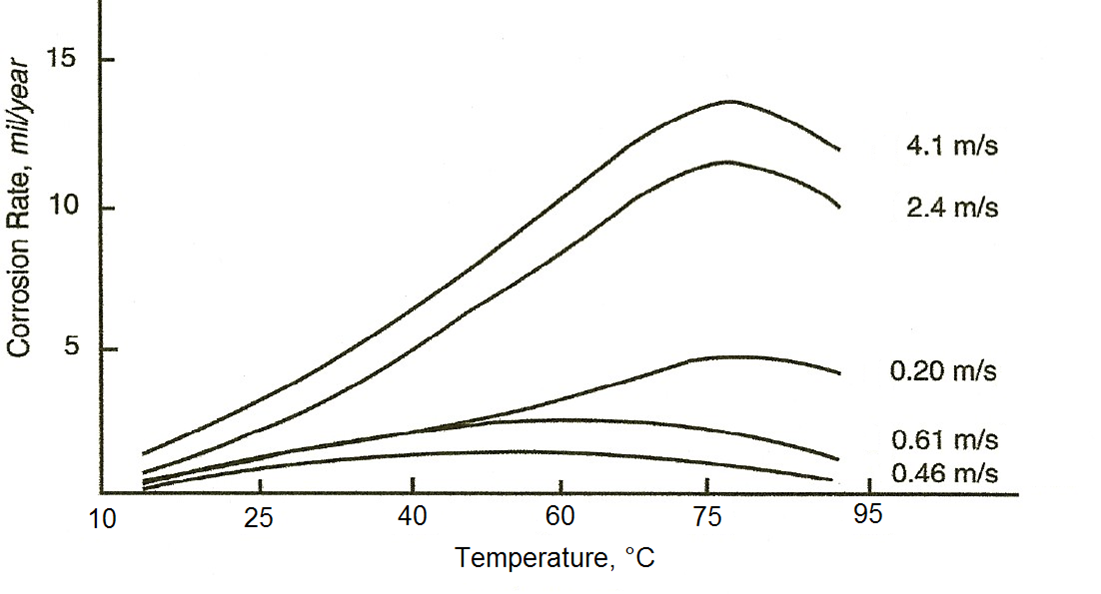
- Düşük oksijen içeriğine sahip suda (< 2 mg/l O2) metalin kendisi stabildir ve kolayca paslanmaz.
- Yüksek oksijen içeriğine (> 2 mg/l O2) sahip asidik suda (pH < 6), metal, bu koşullar altında en kararlı form olan bakır iyonunu (Cu2+, kuprik iyon) oluşturmak üzere çözünebilir. Bu tür sular bakır çözücüdür.
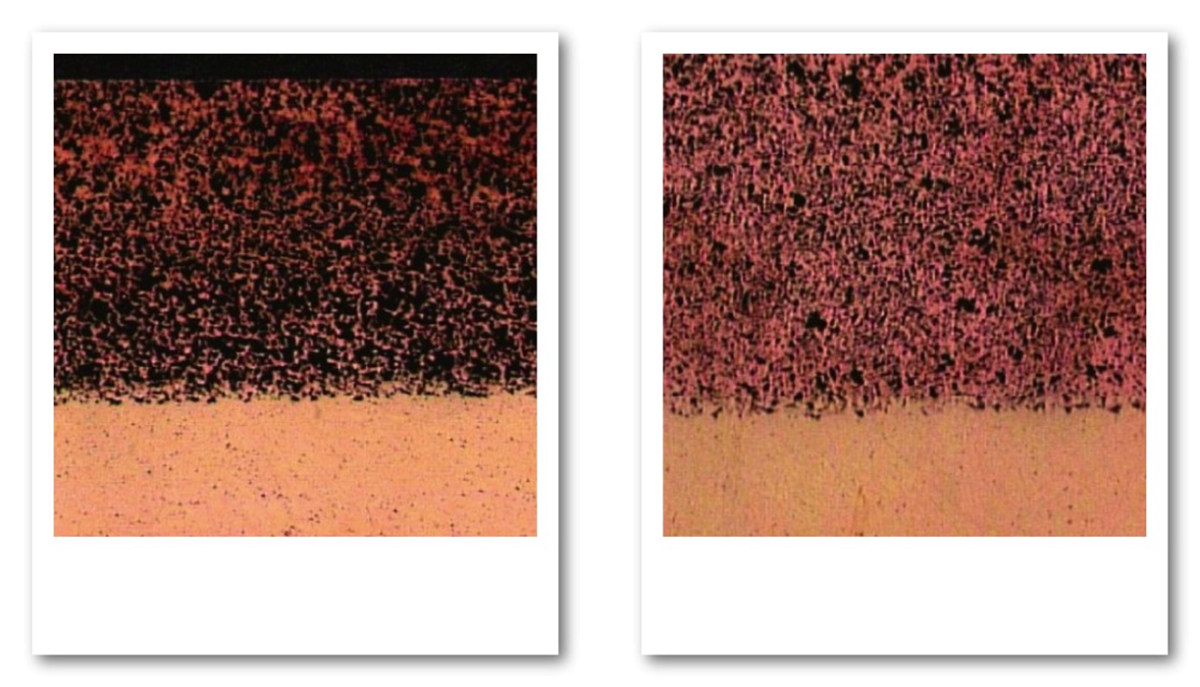
- Yüksek oksijen içeriğine sahip, yaklaşık nötr ila hafif alkali sularda (pH 6 ila 8), metal başlangıçta çözünmeyen bir bakır oksit (Cu2O) tabakası üretebilir.
- Bu magenta kırmızısı ile kahverengi arası korozyon ürünü, bu koşullar altında en kararlı tür olacak ve daha fazla korozyona karşı yarı koruyucu bir tabaka oluşturacaktır.
- Yüksek O2 içeriğine sahip alkali suda (pH > 8,0), bakır bir bakır(II)oksit (CuO) tabakası oluşturabilir.
- Bu siyahtan kahverengiye korozyon ürünü, mevcut koşullardaki en kararlı tür olacak ve daha fazla korozyona karşı yarı koruyucu bir tabaka oluşturacaktır.
Korozyon Türleri
- Pitting
- Tip I – üretim sırasında karbon film oluştuğunda
- Tip II – düşük HCO3 – SO3 oranına sahip sıcak yumuşak suda
- Tip III – çok nadir, düşük alkali içeren sert sularda meydana gelir.

- Erozyon

- SCC Amonyağa Maruz Kalan

- Çinkosuzlaştırma
- Dealloying
- Fatigue
- MIC

1 Comment
I’m extremely impressed with your writing abilities and also with the structure on your blog.
Is that this a paid subject matter or did you customize it yourself?
Either way stay up the excellent high quality writing,
it is uncommon to look a great weblog like this one
these days. Instagram Auto follow!